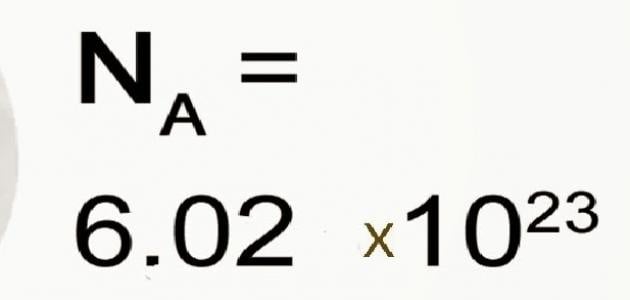محتويات
التعريف بعدد أفوجادرو
عدد أفوجادرو يُطلق عليه أيضاً اسم ثابت أفوجادرو، هو أحد الثوابت المستخدمة في علم الكيمياء والفيزياء، وسمّى بهذا الاسم نسبةً للعالم الذي أوجده. ويمثّل عدد أفوجادرو عدد ذرّات الكربون -12 في 12 غرام من الكربون -12، والذي يعادل العدد 6.022×1023 تقريباً.[١]
وتمّ اختيار عنصر الكربون -12 لحساب العدد لأنّه يمكن قياس كتلته بشكلٍ دقيق، حيث إنّ وزن المول الواحد من عنصر الكربون -12 المُقاس باستخدام مقياس الكلتة الموليّة الافتراضي هو 12.000 وقد تمّ الحصول على هذا العدد عن طريق تقسيم كتلة الذّرة الحقيقيّة على واحدة قياسيّة للكتل الذريّة.[١]
تمّ ابتكار عدد أفوجادرو لأنّ عمليّة التعامل مع الذرّات صغيرة الحجم عمليةً صعبةً جداً ومن الممكن أن تكون مستحيلة، فالذّرات لا ترى بالعين المجردّة أو المجاهر العلميّة، لذلك يُصعب دراستها باستخدام المقاييس العاديّة، لذلك تمّ التفكير في التعامل مع عدد معين من الذرات الخاصّة بعنصر محدد لتسهيل حساب كميّات الذرّات.[١]
علاقة المول بعدد أفوجادرو
إنّ المول هو وحدة لقياس كميّة المادّة في علم الكيمياء، وتعتبر وحدة أساسية حسب النظام العالمي للوحدات، وهي واحدة من الوحدات المستخدمة لقياس كميّة فيزيائيّة، ويعرف المول أيضاً بأنّه الكتلة الذريّة أو الجزيئيّة للمادّة ويمكن التعبير عنه بالغرام، كما يعبّر عن كميّة المادّة التي تحتوي على نفس عدد الجسميات الموجودة في غرام واحد من عنصر الكربون، وفي حالة ذكر المول يجب التفريق ما إذا كان نوع جسميات المادّة ذرّات، أو جزيئات، فإذا كانت ذرّات نقوم بحسابها باستخدام العدد الذرّي، وإذا كانت جزيئات نحسب المول باستخدام الوزن الجزيئي.[٢]
هناك علاقة وثيقة بين المول وعدد أفوجادرو، حيث إنّ عدد الذّرات أو الجزيئات التي توجد في 1 مول من المادّة يساوي عدد أفوجادرو. فعلى سبيل المثال إنّ 1 مول من عنصر الألمونيوم فيه عدد ذرّات كما في 1 مول من عنصر الكربون، وتمّ تحديد عنصر الكربون لأنّه العنصر المعتمد في تحديد عدد أفوجادرو.[٢]
يمكن حساب كميّة المادّة رياضياً باستخدام الخطوات التالية:[٢]
- حساب عدد المولات وهو يساوي مقدار الكتلة مقسوماً على الكتلة المولية.
- حساب كميّة المادّة وهي تساوي عدد المولات مقسوماً على عدد الجزيئات.
أهمية عدد أفوجادرو
تكمن أهمية عدد أفوجادرو في أنه وحدة قياس تبسيطية يستعملها الكيميائِيُّونَ والفيزيائِيَّونَ في حساباتهم، فرقم أفوجادرو يتيح لهم كتابة كتلة مول واحد من المادة بأعداد صغيرة وبوزن جزيئي صغير، كما أنّه يمكّنهم أيضًا من كتابة النسب بين المواد المتفاعلة والمواد الناتجة في المعادلات الكيميائية، وهذا يبسط العمليات الحسابية بشكل كبير.[٣]
أي يمكن عد هذا الرقم كجسر بين الأرقام الضخمة للجزئيات وبين الوحدات المستخدمة كالغرام، فمن دون هذا الرقم لا يمكن حساب كتلة المول الواحد لكل عنصر، إلا بكتابة عدد الجزئيات الضخم، وهذا سوف يصعب الحسابات والتجارب.[٣]
كيفية حساب عدد الذرات باستخدام عدد أفوجادرو
يمكن حساب عدد الذرات باستخدام عدد أفوجادرو كما يأتي:[٤]
- أولاً حساب عدد الذرات وفقاً للقانون الآتي:
عدد الذرات = عدد المولات × عدد أفوجادرو
- وبما أنّ عدد أفوجادرو هو عدد ثابت، لذلك يجب إيجاد وحساب عدد المولات فقط:
عدد المولات = الكتلة (غرام) / الكتلة المولية للمادة (غرام/ مول)
- تُحسب الكتلة المولية إن لم تُعطى في السؤال، من خلال ضرب عدد ذرات العنصر بالكتلة الذرية له والمأخوذة من الجدول الدوري، وعلى سبيل المثال تحسب الكتلة المولية لعنصر O2 من خلال ضرب عدد الذرات (2) بالكتلة الذرية التي تساوي 16 للأكسجين (من الجدول الدوري)، لتكون الكتلة المولية له 32 غرام/مول.[٥]
- وبعد ايجاد عدد المولات، يتبقى التعويض في قانون عدد الذرات.[٤]
أمثلة حسابية على حساب عدد الذرات باستخدام عدد أفوجادرو
فيما يأتي بعض الأمثلة على حساب عدد الذرات باستخدام عدد أفوجادرو:
احسب عدد الذرات الصوديوم الموجودة في 2 مول من كبريتات الصوديوم Na2SO4
الحل:
- لحساب عدد الذرات الصوديوم الموجودة في 2 مول من كبريتات الصوديوم Na2SO4، يجب أولاً حساب عدد ذرات الصوديوم في 1 مول من كبريتات الصوديوم، ثم ضربها بـ 2، كالآتي:
- 1 مول من كبريتات الصوديوم يحتوي على 2 مول من الصوديوم، أي أنّ 2 مول من كبريتات الصوديوم يحتوي على 4 مول من الصوديوم.
- عدد ذرات الصوديوم = عدد المولات × عدد أفوجادرو
- عدد ذرات الصوديوم = 4 × 6.022× 1023 = 24.08 × 1023 ذرة
احسب عدد الذرات الكالسيوم الموجودة في 2 مول من عنصر الكالسيوم؟
لحساب عدد الذرات الموجودة في 2 مول من الكالسيوم Ca، يجب اتباع الخطوات الآتية:
- عدد ذرات الكالسيوم Ca = عدد مولات الكالسيوم Ca × عدد أفوجادرو
- عدد ذرات الكالسيوم = 2 × 6.022 × 1023
- عدد ذرات الكالسيوم = 12.04 × 2310 ذرة
يمثّل عدد أفوجادرو عدد الجزيئات الموجودة في مول من أي مادة، حيث قدّم ذلك العالم الايطالى اميديو أفوجادرو في عام 1811 م، إذ ابتكر عدد أفوجادرو لأنّ التعامل بالحساب مع الذرّات صغيرة الحجم صعب جدًا، ومن الممكن أن يكون مستحيلًا، فالذّرات لا تُرى بالعين المجردّة أو المجاهر العلميّة، لذلك يُصعب دراستها باستخدام المقاييس العاديّة.
المراجع
- ^ أ ب ت JONATHAN ATTEBERRY, "What is Avogadro’s number?"، science.howstuffworks.com, Retrieved 13-7-2018. Edited.
- ^ أ ب ت "The Mole and Avogadro's Constant", chem.libretexts.org, Retrieved 13-7-2018. Edited.
- ^ أ ب Anne Helmenstine (10/5/2021), "what is avogadros number definition and importance", Science Notes, Retrieved 7/10/2021. Edited.
- ^ أ ب " molar mass ", lumen learning, Retrieved 7/10/2021. Edited.
- ↑ "molecular weight of O2", webqc.org, Retrieved 18/11/2021. Edited.